
NEWS
新闻中心Scroll
行业资讯|诺贝尔生理学奖,或将为免疫治疗开启新方向
发布时间: 2019-10-18
阅读次数:1,797次

2019年诺贝尔生理学或医学奖授予了小威廉·G·凯林(William G. Kaelin Jr.)、彼得·J·拉特克利夫爵士(Sir Peter J. Ratcliffe)和格雷格·塞门扎(Gregg L. Semenza),以表彰他们发现细胞感知和适应环境含氧量的相关机制。

氧气约占地球大气的五分之一,是动物生命不可或缺的物质。动物细胞内的线粒体会对氧气加以利用,将食物转化为有用的能量。早在上个世纪,我们就发现与颈两侧的大血管相邻的颈动脉体含有特殊的细胞以感知血液中的氧含量。然而,我们除了在颈动脉体控制下可以对低氧水平做出迅速适应以外,还有一些其他的生理适应机制。在低氧情况下,一个关键的生理反应便是促红细胞生成素(EPO)水平的升高,这种激素会增加红细胞的生成。
那么氧含量是如何控制这一过程的?
格雷格·塞门扎(Gregg L. Semenza)通过研究EPO基因,发现位于EPO基因旁的某些特定DNA片段能调节低氧情况下的一些反应。
彼得·J·拉特克利夫爵士(Sir Peter J. Ratcliffe)也研究了EPO基因的氧气依赖调节,他也发现氧气感应机制不仅存在于产生EPO的肾脏细胞中,还存在于几乎所有组织中。
格雷格·塞门扎(Gregg L. Semenza)在肝细胞中发现了一种蛋白质复合物,这种物质会以一种依赖于氧气的方式与DNA片段结合。他将这种复合物称为缺氧诱导因子(Hypoxia Inducible Factor,HIF)。
从1995年起, Semenza开始对HIF展开广泛研究。通过纯化蛋白的氨基酸序列分析以及随后的cDNA克隆证明HIF自身是异源二聚体,由两个不同基因的产物组成。一个是新发现的,对氧气敏感的部分,被塞门扎命名为HIF-1α;另一个是先前已知的,恒常表达且不受氧调节的蛋白ARNT。
当氧含量低(缺氧)的时候,HIF-1α被保护住不会降解,并在细胞核里聚集。它和ARNT相作用,并结合到特定DNA序列的缺氧调控基因(HRE)上,如图(1)。
在正常的氧气水平下,HIF-1α会由蛋白酶体快速降解,如图(2)。氧气通过为HIF-1α增加羟基(OH)调控了这一降解过程,如图(3)。然后VHL蛋白就可以识别HIF-1α并组成一个复合体,根据氧气浓度决定是否使它降解。
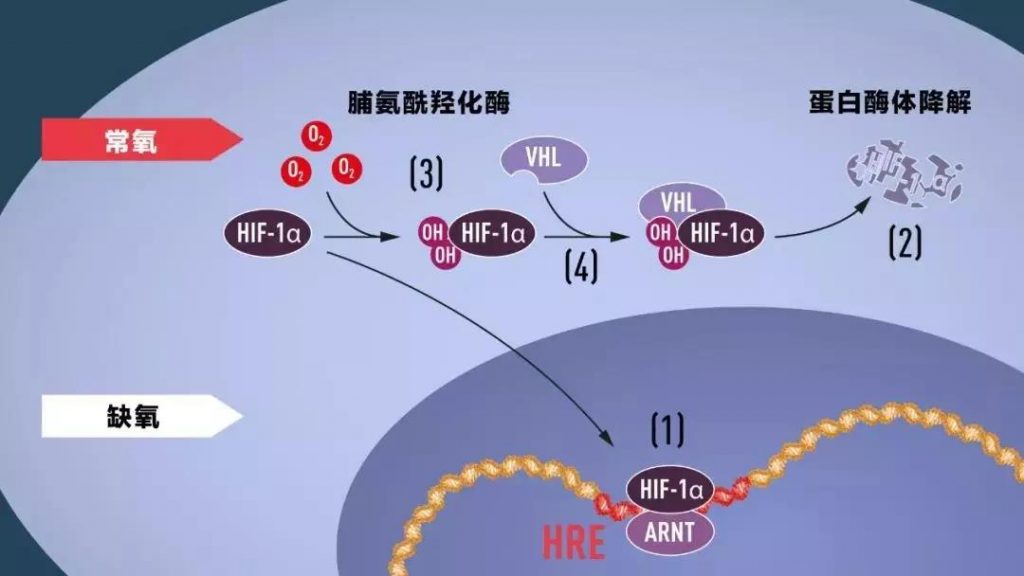
当氧含量很高时,细胞中的HIF-1α含量很少。在这种情况下,蛋白酶体会降解HIF-1α,一种名为泛素的肽会被添加到HIF-1α蛋白质上。泛素是蛋白酶体降解蛋白的标记。接下来的一个核心问题就是,泛素是如何以一种氧依赖性的方式与HIF-1α结合的。
此外,癌症研究者小威廉·G·凯林(William G. Kaelin Jr.)当时正在研究一种遗传性的综合征——希佩尔-林道综合征(VHL,von Hipple-Lindau)。这种遗传性疾病会导致遗传了VHL突变的家庭患某些癌症的风险显著增加。
Kaelin证明VHL基因编码了一种可以预防癌症的蛋白质。他还发现,缺乏正常VHL基因的癌细胞所表达的低氧调节基因水平高于异常。但当VHL基因被重新引入癌细胞时,含氧量水平又会恢复到正常。氧通过羟基结合到HIF-1α的过程来调节HIF-1α的降解。VHL蛋白可以识别并形成一个包含HIF-1α的复合体,导致其以一种依赖氧气的方式降解。此后,彼得·J·拉特克利夫爵士(Sir Peter J. Ratcliffe)于1999年证明了:VHL可以与HIF-1α相互作用,并且它是HIF-1α在正常氧气水平下降解所必需的,将HIF-1α与VHL联系在了一起。最后,凯林和拉特克利夫爵士的研究组同时发现,VHL对HIF-1α的调节取决于HIF-1α的羟基化,这是一种共价修饰,其本身依赖于氧。

三位诺奖得主的研究成果让我们对不同的氧气水平如何调节基础的生理过程有了更深的了解。氧气感知机制能使细胞可以调节自己的新陈代谢以适应低氧水平。而这一研究也为癌症和免疫治疗带来了新的契机。
在实体肿瘤中,阻碍免疫细胞工作最大的难点之一就是肿瘤会在局部形成适合自己生存的肿瘤微环境,而这个微环境的一个重要特点就是——缺氧。这主要是因为肿瘤细胞相对来说复制更加迅速,也就意味着需要消耗更多能量,但是细胞供给的能量就只有那么多,因此就会造成缺氧的情况出现。这时HIF基因就会开始行动,它会认为人体是处于缺氧的状态,然后对机体进行调整,新生更多的血管,这也是癌细胞的狡猾之处——它可以利用人体内本来正常的生理机制来促进自己的生长。癌细胞通过这一途径建立自己的能量供给——促进新生血管为自己提供更多的氧气以及血管中的营养物质,并不断地为发展做充足的准备。可以说:低氧或缺氧是许多肿瘤生长过程的决定因素。
另外一方面,氧气的感知对免疫细胞的功能也有很重要的影响,它可以决定免疫细胞是否能够发挥出应有的杀灭作用。人体内的T细胞是最重要的免疫细胞之一,它有一个很重要的功能,就是可以针对性地杀灭癌细胞,这也使其成为攻克癌细胞的主力军。但是不论是何种技术,其本身都是建立在T细胞功能的基础上。一项在《Nature Immunology》发布的最新研究显示:通过T细胞所处环境中氧气和营养的改变可以影响T细胞的功能,从而让T细胞发挥更加强大的作用。他们发现:当T细胞开始工作的时候,比如识别到入侵的细菌或者病毒,就会开启氧气感知通道和养分汲取的关键通道,这样T细胞就可以更好地发挥杀灭作用。反过来亦然,这也是为什么T细胞进入到肿瘤微环境之后杀伤作用就会降低的原因。
抑制HIF功能也有许多应用:HIF 水平的增加可见于许多癌症以及一些心血管疾病,包括脑卒中、心脏病发作和肺部高压。从反面来说,通过药物提升HIF功能可能有助于治疗一系列疾病,因为HIF对许多生理过程都必不可少,比如免疫功能、软骨形成和伤口愈合。
现在只是本届诺贝尔奖发现被应用的开始,更明显的事实是,细胞、组织和生物体对氧气的反应,是动物所具有的最重要的生理适应之一。对于免疫治疗而言,不论是癌细胞的发生发展还是T细胞发挥作用,都和氧气感知基因有着诸多联系,而随着基础机制的研究深入,免疫治疗也将发挥更好的作用。
参考资料:
1、From sleeping cell to assassin—how immune cells work.
2、Quantitative analysis of T cell proteomes and environmental sensors during T cell differentiation.
3、The Nobel Prize in Physiology or Medicine 2019.
—— end ——

