
NEWS
新闻中心Scroll
人体的始祖细胞
发布时间: 2020-09-04
阅读次数:2,298次
什么是造血干细胞?
造血干细胞是指尚未发育成熟的细胞,是所有血细胞和免疫细胞的起源,它可以分化为红细胞、白细胞和血小板,还可跨系统分化为各种组织细胞,因此是多功能干细胞,医学上称其为“万用细胞”,也是人体的始祖细胞。

·造血干细胞有两个重要特征:
其一,高度的自我更新或自我复制能力;
其二,可分化成所有类型的血细胞。
造血干细胞采用不对称的分裂方式:由一个细胞分裂为两个细胞。其中一个细胞仍然保持干细胞的一切生物特性,从而保持身体内干细胞数量相对稳定,这就是干细胞自我更新。而另一个则进一步增殖分化为各类血细胞、前体细胞和成熟血细胞,释放到外周血中,执行各自任务,直至衰老死亡,这一过程是不停地进行着的。
·造血干细胞移植的意义
造血干细胞移植是现代生命科学的重大突破。造血干细胞移植可治疗恶性血液病,部分恶性肿瘤,部分遗传性疾病等近百种致死性疾病。包括急性白血病、慢性白血病、骨髓增生异常综合征、造血干细胞疾病、骨髓增殖性疾病、淋巴增殖性疾病、巨噬细胞疾病、遗传性代谢性疾病、组织细胞疾病、遗传性红细胞疾病、遗传性免疫系统疾病、遗传性血小板疾病、浆细胞疾病、地中海贫血、非血液系统恶性肿瘤、急性放射病等。
因为有了造血干细胞移植技术,世界各地成千上万患有以上疾病的患者,重新燃起了生命的希望。
·造血干细胞的移植现状
1988年法国的Gluckman教授在国际上率先成功采用脐血造血干细胞移植,救治了一名贫血患儿,标志着脐带血造血干细胞移植时代的开启。
全球现每年约进行6万例骨髓移植术,其中使用自体和同种异体造血干细胞完成骨髓移植术的患者人数分别为近3.5万和2.5万例。造血干细胞的来源主要包括骨髓、外周血和脐带血。如今,“骨髓移植”已渐渐被“外周血造血干细胞移植”代替。也就是说,现在捐赠骨髓已不再抽取骨髓,而只是“献血”了。脐带血是胎儿娩出断脐后残留在脐带和胎盘中的血液,富含造血干细胞,可用于治疗急、慢性白血病和某些恶性肿瘤等多种重大疾病。
·造血干细胞研究进展
1.造血干细胞通过保持对以前感染的记忆来提高免疫反应
在一项新的研究中,来自法国、德国和以色列的研究人员发现造血干细胞的一个令人吃惊的特性:它们不仅确保血细胞的持续更新,而且还能够记住以前的感染经历,从而在未来引发更快更有效的免疫反应。这些发现应当对未来的疫苗接种策略产生重大影响,并且为表现不佳或反应过度的免疫系统开发新疗法铺平道路。相关研究结果近期发表在Cell Stem Cell期刊上,论文标题为“C/EBPβ-Dependent Epigenetic Memory Induces Trained Immunity in Hematopoietic Stem Cells”。论文通讯作者为Michael Sieweke博士和Sandrine Sarrazin博士。
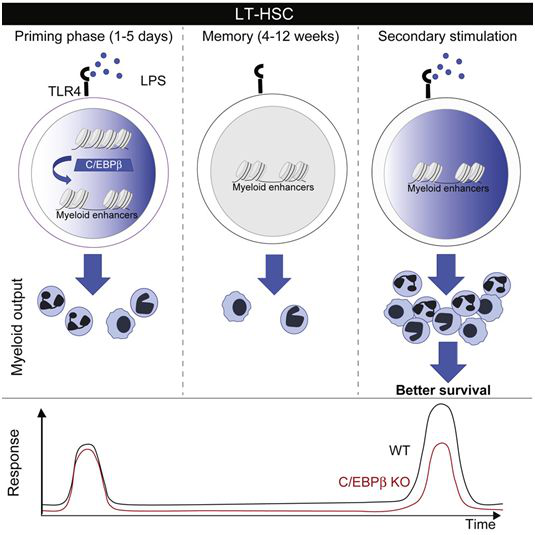 图片来自Cell Stem Cell, 2020, doi:10.1016/j.stem.2020.01.017
图片来自Cell Stem Cell, 2020, doi:10.1016/j.stem.2020.01.017
直到十年前,普遍流行的观点是HSC是非特化细胞,对诸如感染之类的外部信号视而不见。只有它们的特化子细胞才能感知这些信号并激活免疫反应。但是Sieweke实验室和其他实验室在过去几年的研究工作已证实了这种观点是错误的,并表明HSC实际上可以感知外部因素,以“按需”特异性产生抵抗感染的免疫细胞亚型。除了它们在紧急免疫反应中的作用外,HSC在应对反复感染事件中的功能仍是未知的。已知免疫系统具有记忆功能,这允许它更好地应对再次入侵的传染原。如今,这项新的研究确立了HSC在这种记忆中的核心作用。
Sarrazin说,“我们发现,如果HSC以前暴露于脂多糖(一种模拟感染的细菌分子),那么它们可以促进更快更有效的免疫反应。”Sieweke解释了他们如何发现这种记忆存储在这些干细胞中:“首次暴露于脂多糖会导致一些标记在HSC的DNA上堆积,而且就堆积在对免疫反应至关重要的基因周围。DNA上的这些标记就像书签一样,可以确保当再次遭受相同病原体感染时,这些基因容易被找到、访问和激活以快速产生反应。”
这些作者进一步探索了记忆是如何刻在DNA上的,并发现C/EBPb在其中起着重要作用,描述了这种因子的新功能,此外,该功能对于紧急免疫反应也很重要。总之,这些发现应当有助于改善对免疫系统的调节或开发更好的疫苗接种策略。

2.造血干细胞有助于提高骨髓移植效率
根据2月27日发表在《Cell Stem Cell》杂志上的一项研究,西奈山的研究人员发现了一种增强造血干细胞效力的方法,这可能为新的骨髓移植方法打开了大门。
 图片来源:Wikipiedia
图片来源:Wikipiedia
骨髓移植可以治愈许多血液疾病和实体瘤,而造血干细胞的稀缺严重限制了骨髓移植。西奈山研究小组的报告称,通过调控溶酶体周围的代谢活性,可以使造血干细胞在骨髓移植中的功效提高90倍以上。
“造血干细胞一旦在培养皿中培养,就会失去干细胞潜能,这限制了它们在实验室培养中易于繁殖的能力,”医学发展与再生生物学教授Saghi Ghaffari说道“为了使这些干细胞保持最佳效能,它们不应该时刻处于分裂状态,而是应处于休眠或静止状态。溶酶体是这些细胞休眠的关键。我们进一步了解到,抑制溶酶体活性可增强干细胞的静止性和效力,并可能具有治疗价值。”
通过在小鼠中进行研究,西奈山的科学家使用了有效而又特异的溶酶体抑制剂,可降低溶酶体的酸度和细胞中氨基酸的释放。最终结果是将具有活化溶酶体的干细胞恢复到静止状态。这项研究进一步发现,抑制糖酵解反应还可以增强造血干细胞的静止性和分裂潜力。
以上部分资料来源与网络
—— end ——
-文中部分图片来源于网络,如有侵权请联系我们及时删除-

